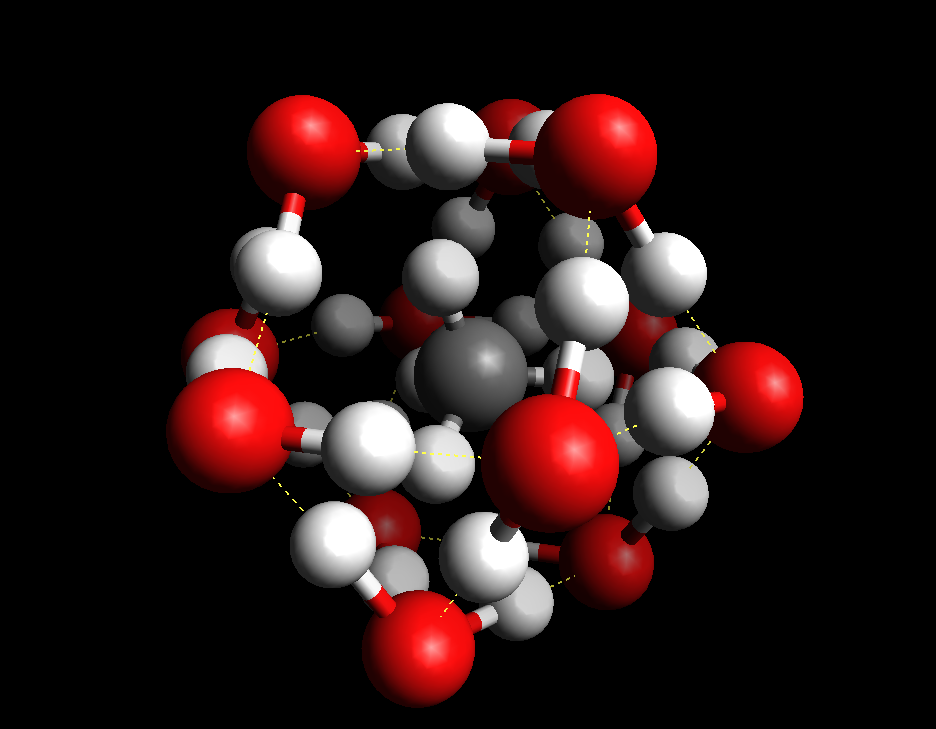
甲烷气水包合物(Methane clathrate),也称作甲烷水合物、甲烷冰、天然气水合物或可燃冰,为固体形态的水于晶格(水合物)中包含大量的甲烷。最初人们认为只有在太阳系外围那些低温、常出现冰的区域才可能出现,但后来发现在地球上许多海洋洋底的沉积物底下,甚至地球大陆上也有可燃冰的存在,其蕴藏量也较为丰富。甲烷气水包合物作为石油、天然气的新时代替代能源而备受期待。
甲烷气水包合物存在于低温高压的环境,在海洋浅水生态圈中是常见的成分,他们通常出现在深层的沉淀物结构中,或是在海床处露出。甲烷气水包合物据推测是因地理断层深处的气体迁移,以及沉淀、结晶等作用,于上升的气体流与海洋深处的冷水接触所形成。
在高压下,甲烷气水包合物在18°C的温度下仍能维持稳定。一般的甲烷气水化合物组成为1莫耳的甲烷及每5.75莫耳的水,然而这个比例取决于多少的甲烷分子“嵌入”水晶格各种不同的包覆结构中。据观测的密度大约...